Пример решенной контрольной работы по химии
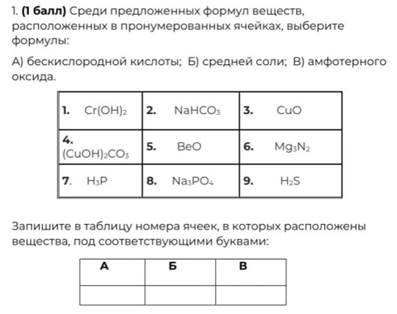
Бескислородные кислоты – класс кислот в состав которых не входит кислород. Из предложенного списка это сероводородная кислота H2S.
Средняя соль – соль образованная катионом металла и кислотным остатком с учетом того, что в кислоте замещены все атомы водорода, в основании – все группы ОН-, то есть в составе соли нет катионов водорода и гидроксогрупп. Из предложенных веществ это фосфат натрия Na3PO4
Амфотерный оксид – оксид который реагирует как с кислотами, так и с основаниями, образуя соответствующие соли.
Из предложенных веществ это оксид бериллия ВеO.
Получаем:
|
А |
Б |
В |
|
9 |
8 |
5 |

а) Данная реакция является реакцией соединения, так как из двух веществ образуется одно, более сложное вещество.
б) Данная реакция не является окислительно-восстановительной, так как в ходе реакции ни один элемент не изменяет степени окисления.
в) Данная реакция является необратимой, так как гидроксид кальция является малорастворимым веществом
г) Данная реакция является экзотермической, так как в ходе реакции выделяется большое количество теплоты.

Скорость реакции зависит от температуры, чем выше температура тем больше скорость реакции; зависит от концентрации веществ, чем выше концентрация тем выше скорость; зависит от степени измельчения (поверхности раздела) твердых веществ. Чем больше поверхность, то есть чем больше произведено измельчение твердого вещества тем выше скорость. Так же зависит от катализатора.
Исходя из этого видно, что правильными вариантами будут 2 и 5.

Лампочка загорится только в растворах электролитов. К электролитам относят все растворимые соли (сильные электролиты) все растворимые кислоты и основания.
Дистиллированная вода не является электролитом.
Из предложенных веществ электролитами будут
II) раствор поваренной соли, хлорида натрия, который диссоциирует на ионы:
NaCl = Na+ + Cl-
(IV) раствор уксусной кислоты, слабый электролит, частично диссоциирующий:
CH3COOH = CH3COO- + H+
V) раствор каустической соды или гидроксида натрия, сильный электролит, полностью диссоциирующий на ионы:
NaOH = Na+ + OH-
VI) раствор кальцинированной соды или карбоната натрия, который растворим в воде и является сильным электролитом:
Na2CO3 = 2Na+ + CO32-

![]() Дано: Решение
Дано: Решение
С2(Na2SO4; Ba(NO3)2) = 0,65 моль/л При взаимодействии сульфата натрия и нитрата бария
С1(Na2SO4; Ba(NO3)2) = 3,85 моль/л образуется осадок сульфата бария:
t1 = 35 сек Na2SO4 + Ba(NO3)2 → BaSO4↓ + 2NaNO3
t2 = 2 мин Скорость реакции в текущий момент времени равна
![]() v - ? отношению изменения концентрации за промежуток
v - ? отношению изменения концентрации за промежуток
времени:
v = (С1 – С2) / (t2 – t1)
Подставляя все данные. Получаем:
t2 = 2 мин = 120 сек.
v = (3,85 – 0,65) / (120 – 35) = 3,2 / 85 = 0,04 моль/л*сек
