Пример решенной контрольной работы по химии

Решение:
Согласно закону разбавления Оствальда имеем:
![]()
Где ![]() – константа диссоциации кислоты; α – степень диссоциации кислоты; С – концентрация раствора.
– константа диссоциации кислоты; α – степень диссоциации кислоты; С – концентрация раствора.
После подстановки известных величин получаем:
![]()
Ответ: концентрация уксусной кислоты 0,18 моль/л.

Решение:
Смесь гидрофосфата и дигидрофосфата представляет собой фосфатную буферную систему, в которой дигидрофосфат выполняет роль слабой кислоты, гидрофосфат – сопряженного основания.
для фосфатного буфера уравнение Гендерсона-Гассельбаха запишется следующим образом
![]()
где рК – показатель кислотности фосфорной кислоты по второй ступени, рК = 7,2
После подстановки известных величин получаем:
![]()
где ![]() , т.е.
, т.е. ![]()
условие равенства концентраций компонентов буферной системы достигается смешением равных объемов исходных компонентов. Таким образом, для приготовления 100 мл буферной смеси необходимо смешать 50 мл 0,1 моль/л раствора гидрофосфата натрия и 50 мл 0,1 моль/л дигидрофосфата натрия.

Решение:
Уравнение реакции сгорания ацетилена:
С2Н2 + 5/2 О2 = 2СО2 + Н2О +1300 кДж
Согласно следствиям из закона Гесса изменение энтальпии химической реакции (тепловой эффект реакции) равен:
ΔHр-ции=ΣHкон–ΣHисх кДж/моль
ΔHр-ции = 2*ΔH0CО2+ΔH0Н2O—ΔH0 C2Н2 -5/2* ΔH0О2
Откуда теплота образования ацетилена равна:
ΔH0 C2Н2 =2*ΔH0CО2+ΔH0Н2O -5/2* ΔH0О2 - ΔHр-ции
ΔH0 C2Н2 =2*(-393,5)+(-286)-5/2*0-(-1300) =+227 кДж/моль
Ответ: +227 кДж/моль

Решение:
Выражение для скорости химической реакции:
V=k[NO]2[O2]
Согласно уравнению Клапейрона 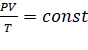
Уменьшение давления в системе равносильно увеличению объема системы, а соответственно, уменьшению концентрации компонентов в 5 раз. В результате получаем:
V’=k[1/5NO]2[1/5O2] = 1/125 *V
Скорость реакции уменьшится в 125 раз.
Ответ: уменьшится в 125 раз.

Ответ:
Ионные радиусы s-элементов существенно меньше металлических, что связано с потерей валентного электрона. Они возрастают от лития к цезию и от бериллия к радию. Размеры гидратированных катионов изменяются в противоположном направлении, что объясняется в рамках простейшей электростатической модели. Наименьший по размеры катион лития лучше катионов остальных s-элементов притягивает к себе полярные молекулы воды, образуя наиболее толстую гидратную оболочку. По этой причине многие соли лития выделяют из водных растворов в виде кристаллогидратов.
Ответ:
Процесс биосинтеза фосфолипидов (ФЛ) связан с обновлением клеточных мембран. Первые стадии синтеза ФЛ совпадают с синтезом триацилглицерида до фосфатидной кислоты, а из нее — диглицерида. Но для дальнейшего синтеза ФЛ необходимо азотсодержащее соединение, которое предварительно активируется. В этом принимают участие два нуклеозидтрифосфата: АТФ и ПТФ. Аминоспирт преобразуется в ЦДФ- производное в два этапа:
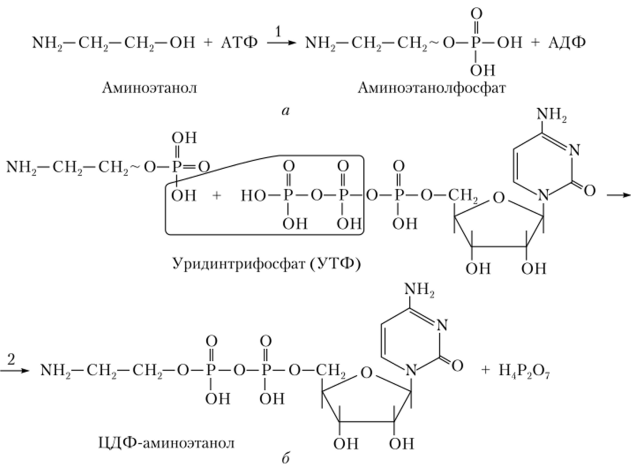
Активирование аминоспирта: а — фосфорилирование; б — образование ЦДФ-производного
Далее на свободную ОН-групну диацилглицерида переносится фосфорилированный аминоснирт из ЦДФ-производного
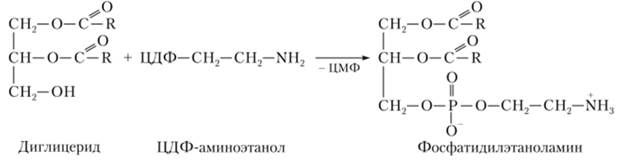
В процессах пищеварения все омыляемые липиды (в том числе фосфолипиды) подвергаются гидролизу на составные части. Фосфолипиды расщепляются полностью или частично под действием гидролитических ферментов - специфических фосфолипаз. Продуктом полного гидролиза фосфолипидов являются: глицерин, высшие жирные кислоты, фосфорная кислота и азотистые основания.
Все фосфолипазы - кальцийзависимые ферменты.
![]()
Ответ:
При соединении двух молекул аминокислот образуется дипептид, трёх - трипептид и т. д. Пептиды, в состав молекул которых входит 10—20 аминокислотных остатков, называются олигопепти́дами; при большем количестве аминокислотных остатков пептиды называются полипепти́дами. В состав молекул полипептидов могут также входить неаминокислотные остатки, например углеводные. К пептидной цепи может присоединяться неограниченное количество аминокислотных остатков, что приводит к образованию веществ с очень большой молекулярной массой - белкам.
Пептидная связь образуется между двумя молекулами аминокислот за счет отщепления молекулы воды. Основным свойством пептидов является их способность к гидролизу - полному или частичному. В результате гидролиза происходит расщепление пептидной цепи. Полный гидролиз приводит к образованию смеси -аминокислот, частичный - к образованию смеси пептидов с меньшей молекулярной массой. Гидролиз пептидов может осуществляться как в кислой, так и в щелочной среде, а также ферментативно. В кислой и щелочной средах образуются соответствующие соли аминокислот. Ферментативный гидролиз может происходить селективно, то есть с расщеплением пептидной цепи только в определённых участках полипептидной цепи. Качественной реакцией на пептиды, как и на аминокислоты, является нингидриновая реакция. Кроме того, пептидную связь можно обнаружить с помощью биуретовой реакции: при действии солей меди(II) в щелочном растворе на все соединения, содержащие пептидную связь, возникает фиолетовое окрашивание.
Биологическое значение пептидов связано с тем, что многие из них проявляют биологическую активность и регулируют процессы жизнедеятельности. Некоторые пептиды являются гормонами, например: трипептид глутатион, который состоит из остатков глицина, цистеина и глутаминовой кислоты, вазопрессин и окситоцин, состоящие из девяти аминокислотных остатков. Вазопрессин повышает кровяное давление, а окситоцин стимулирует выделение молока молочными железами.
Белки - биологически активные вещества, многие из них являются лекарственными препаратами. Белки используются также для создания тест-систем, позволяющих диагностировать целый ряд заболеваний, в том числе инфекционных, онкологических, генетических и т. д.. Многие вакцины и сыворотки имеют белковую природу и применяются для профилактики инфекционных заболеваний.
Благодаря белкам организм приобрел возможность двигаться, размножаться, расти, усваивать пищу, реагировать на внешние воздействия и т. д.
Белки - это природные высокомолекулярные соединения (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков -аминокислот, соединённых пептидной связью. В состав белков входит более 50 α-аминокислотных остатков. В состав белков входит 20 различных аминокислот, что при различных комбинациях аминокислот обусловливает огромное многообразие белков.

Ответ:
Полисахариды — это природные высокомолекулярные вещества, представляющие собой продукты конденсации большого числа молекул моносахаридов.
Иногда их называют несахароподобными за отсутствие сладкого вкуса. По виду мономерных звеньев полисахариды подразделяют на гомополисахариды, образованные одинаковыми моносахаридами, и гетерополисахариды, образованные разными моносахаридами.
Важнейшие природные полисахариды — крахмал, гликоген и клетчатка относятся к гомополисахаридам.
Крахмал — широко распространенный в природе полисахарид. По своему составу крахмал неоднороден, он представляет собой смесь двух полисахаридов: амилозы (13—30%) и амилопектина (70—85%).
Амилоза — линейный полимер, который скручен в спираль, а-глюкозные остатки в нем связаны 1,4-кислородными мостиками. В каждой молекуле амилозы содержится 200—400 остатков глюкозы.
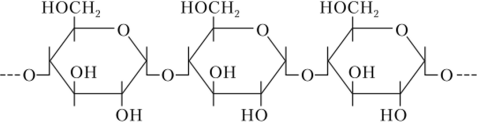
Фрагмент молекулы амилозы
Амилопектин подобно амилозе содержит 1,4-а-связанные остатки глюкозы, но, кроме этого, имеются еще поперечные 1,6-кислородные мостики между некоторыми глюкозными остатками. В результате цепи амилопектина сильно разветвлены и имеют шаровидную форму. Полимер амилопектипа содержит 600—6000 глюкозных остатков.
Амилоза растворима в холодной воде, а амилопектин — только в горячей, поэтому крахмал не растворим полностью в холодной воде, но в горячей он легко набухает, образуя вязкий коллоидный раствор — крахмальный клейстер.
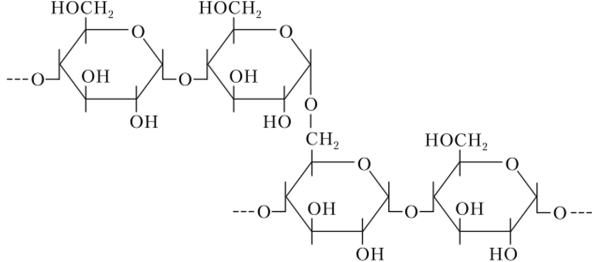
Фрагмент молекулы амилопектина
Крахмал – главное запасное питательное вещество растений, основной источник резервной энергии в растительных клетках.
Остатки глюкозы в молекулах крахмала соединены достаточно прочно и в то же время под действием ферментов легко могут отщепляться, как только возникает потребность в источнике энергии.
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах.
Ответ:
К пуриновым азотистым основаниям относят аденин и гуанин.
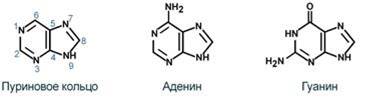
На основе азотистых оснований синтезируются нуклеозиды, представляющие собой комбинацию азотистого основания и рибозы (или дезоксирибозы).
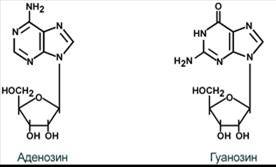
Присоединением одного, двух или трех остатков фосфорной кислоты к нуклеозиду достигается образование соответственно нуклеозид(моно-, ди-, три)фосфатов – нуклеотидов.
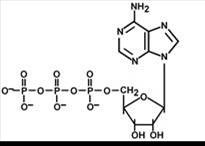 АТФ (аденозинтрифосфат)
АТФ (аденозинтрифосфат)
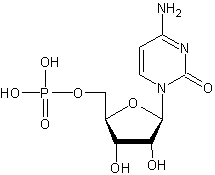
Перечисленные в задании ТМФ. УМФ, дЦМФ, ЦМФ являются производными пиримидиновых оснований:
ТМФ
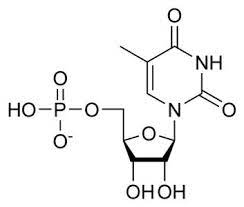
УМФ
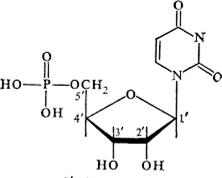
дЦМФ
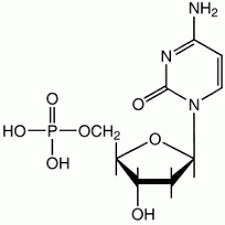
ЦМФ
Ответ:
Полиэлектролиты — это полимеры, макромолекулы которых содержат ионогенные функциональные группы, способные к электролитической диссоциации.
При диссоциации макромолекулы полиэлектролитов распадаются на макроионы и низкомолекулярные противоионы. Как и низкомолекулярные электролиты, по степени диссоциации полиэлектролиты подразделяют на слабые, в которых диссоциации подвергается лишь часть ионогенных звеньев, и сильные, которые диссоциируют практически полностью. По характеру образующихся при диссоциации продуктов полиэлектролиты классифицируют как поликислоты, полиоснования, полисоли и полиамфолиты.
В зависимости от силы иоиогенных групп при определенном pH заряды скомпенсированы, такое состояние молекулы называют изоэлектрическим, а соответствующее ему значение pH — изоэлектрической точкой (ИЭТ).
Поскольку pH оказывает сильное воздействие на структуру (конформации) макромолекул ВМС-полиэлектролитов, то и их свойства (вязкость, степень набухания, оптическая плотность) изменяются в зависимости от pH:
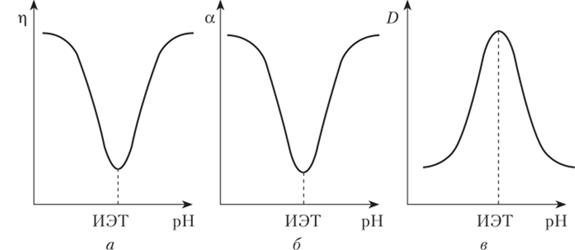
Определение ИЭТ: а — по зависимости вязкости раствора от pH; б — по зависимости степени набухания от pH; в — по зависимости оптической плотности раствора от pH
В изоэлектрическом состоянии молекула белка имеет структуру плотного клубка или глобулы, что затрудняет набухание, препятствует прохождению света через раствор, снижает вязкость и сопротивление течению жидкости. При выпрямлении молекул в областях pH больше или меньше ИЭТ возрастает вязкость, упрощается набухание, снижается оптическая плотность.
Заряд и форма макромолекулы полиэлектролита зависят от pH среды. Зависимость структуры белка от pH используется для определения ИЭТ.
